GENITALES AMBIGUOS

El nacimiento
de un bebe, es quizás la experiencia más hermosa de toda madre o padre, es una
felicidad tanto para padres como para
la familia. Pero quizás la pregunta que
más se hace a una pareja que tendrá un hijo es ¿será niño o niña?
En épocas
anteriores hasta la llegada de la ecografía, esta era una pregunta que todo
padre se hacía, pero ya con los avances médicos y las técnicas, la mayoría de
los embarazos ya se puede conocer el género del bebe, por medio de la
ecografía, la cual se sabe más o menos a las 20 semanas de gestación.
Muchas personas
dirían ¿Qué fácil es saber si él bebe
que ha de venir será niño o niña con solo una ecografía? parece una pregunta
fácil de responder, pero a veces no es posible saber el género del bebe, como
ocurre al encontrar en un bebe con ambigüedad
sexual, la cual es una patología que afecta a menos de 1% de la
población.
Cuando un
médico, recibe un bebe al cual no es posible designar un género, ya sea
masculino o femenino, será un reto tanto para el personal de salud como para la
familia además de un dolor para sus padres.
“Todo médico o
personal de la salud debe actuar rápidamente para descubrir las enfermedades
que amenazan la vida, confortar a los padres respecto a la situación e iniciar
una valoración que permita pronto señalar el sexo”
El desarrollo
sexual normal, se puede ser considerado en 5 niveles que están estrechamente
relacionados.
·La
determinación sexual del cigoto
·El desarrollo
gonadal: ovarios o testículos
·El proceso de
organización de los conductos internos del aparato sexual masculino y femenino.
·La estructura
de los genitales externos
·La
feminización y masculinización en la pubertad
La determinación sexual

Depende
completamente del componente sexual del gameto masculino en la fecundación,
como se conoce hace varios años el 100% de los gametos femeninos tiene cromosomas x, en cambio los hombres la
mitad de cromosomas son Y , la otra es
X.
En el momento
de la fecundación un espermatozoide fecundara a un ovulo, produciendo un cigoto
cuyo par sexual será XX para una niña y XY para un niño.
La diferenciación gonadal
A finales de la
cuarta semana de gestación, hay un engrosamiento del epitelio celomico del embrión, para generar los pliegues
genitales, los cuales migraran, las
células germinales que son procedentes del saco vitelino., estos son los
pliegues donde se desarrollaran las
futuras gónadas. Estos pliegues están constituidos por una zona cortical a
nivel periférico y otra medular a nivel central.
Esta estructura
es única, bipotencial que estará presenta tanto en embriones masculinos como
femeninos.
Durante la
fecundación cuando el cigoto es XY, se iniciara hacia la semana 4, el
desarrollo testicular a partir de la proliferación de la zona medular y la atrofias de la zona cortical. Cuando el
cigoto es XX, se iniciara una proliferación en la zona cortical y una atrofia
de la zona medular y se producirá el
desarrollo de los ovarios.
Diferenciación de la gónada bipotencial en
ovario o testículo.
La
diferenciación gonadal inicia en la semana 4
y termina en la semana 8 en el varón y días después en la mujer. La
determinación sexual de las gonadas, necesita de procesos moleculares que
lleven a la diferenciación de las estructura sexuales masculinas y femeninas
diferenciación sexual

La
diferenciación testicular normal dependerá del gen SRY, la cual es el motor
inicial e importante en diferenciación sexual
Por medio de
muchas investigaciones se sabe que a finales de la sexta semana de gestación
los cordones sexuales son separados del epitelio superficial por un tejido
denso llamado túnica albugínea, las células que están presentes en los cordones
sexuales o cordones seminíferos están formados por células germinales y
somáticas las cuáles serán las
precursoras de las células de sertoli. En el compartimiento estromatico de las
gónadas se encuentra ubicadas las células de Leydig, además de otras estructuras como los vasos sanguíneos,
nervios, fibroblastos, células mesenquimales y matriz extracelular, en la a
octava semana de gestación las células de Leydig se diferenciaran y comenzaran
a sintetizar testosterona y androstenediona., además de secretar andrógenos,
que son necesarios en el desarrollo de los conductos de Wolff y de los
genitales masculinos.
Las células de
sertoli por otro lado producirán hormona antimulleriana, que será de gran
importancia en la regresión de los conductos de Müller que es
los precursores de la formación de ovoductos y útero en las mujeres.
Diferenciación ovárica
En control de
la diferenciación sexual en las mujeres no es del todo claro ,además de que las
gónadas permanecen indiferenciada pasadas las 7 semanas, por medio de varias
investigaciones se han encontrado genes involucrados en la diferenciación
sexual en embriones XX, entre ellos está el gen WNT4 y FOXL2.
Se conoce que
el Wnt-4 es necesario para la diferenciación ovárica, incluyendo las células
germinales. La presencia de las células germinales es necesaria para la
diferenciación del ovario y la formación de los folículos primordiales.
Diferenciación de sistema de conductos internos o genitales internos
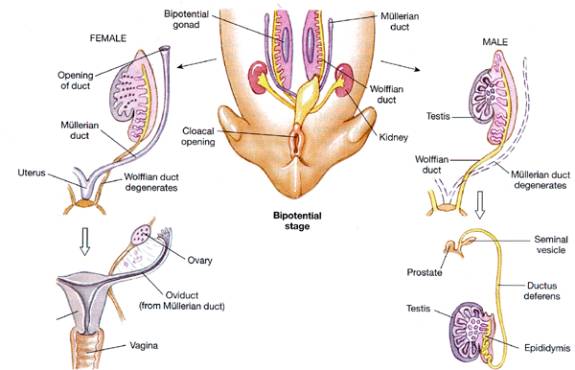
La
diferenciación sexual se refiere a la
diferenciación de los conductos de Wolff o Mϋller en conductos masculinos o
femeninos. Si hay ausencia de los testículos, se desarrollara el conducto de
Müller, este está bajo el control de estímulo de gen WNT4, para formar loas
trompas uterinas, el útero y el tercio superior de la vagina.
Cuando hay
presencia de testículos, las células de sertoli segregan AMH para inhibir el
Conducto de Müller entre la semana 9 y 12, este efecto es mediado por un
receptor específico para AMH.
Otras células
importantes del testículo son las células de Leydig que segregan testosterona
para estimular la diferenciación del conducto de Wolff, que va a dar lugar a la
formación del epidídimo y los conductos deferentes
Pero hay que
saber y conocer que tanto los embriones femeninos como masculinos poseen los
dos sistemas ductales.
Periodo de diferenciación de los genitales
externos
Como pasa en la
diferenciación de las estructuras internas
tanto masculinas y femeninas, en los genitales externos, existe una estructura
primitiva única que se diferenciara
según la acción hormonal.
La estructura
es igual en ambos sexos, en donde habrá un seno urogenital, la presencia de
prominencias labioescrotales , dos pliegues uretrales laterales y un tubérculo
genital
·el tubérculo
genital formara: pene y clítoris
·los pliegues
labio-escrotales se fusionaran por la acción hormonal para formar el escroto y
la piel ventral del pene en el hombre,
en la mujer los pliegues
labio-escrotales no se fusiona y formaran los labios mayores
·los pliegues
uretrales, en los hombres formara la
uretra perineal y peneana y en la mujer
formara los labios menores.
·Seno
urogenital se va a diferenciar en la uretra y porción inferior de la vagina.
·Los genitales
externos tienen una tendencia a la
feminización, el desarrollo femenino es pasivo y se produce en ausencia de las
gónadas, pues no requiere del estímulo hormonal.
·La
masculinización de los genitales externos en el hombre dependerá de la acción de la DHT y esta se deberá producir en el periodo entre
la semana 8 y 12 de la vida fetal, el cual es un periodo crítico de la
diferenciación sexual.
Caracteres secundarios
En este periodo
estará constituido por las características sexuales que van a dar lugar a la
feminización completa en la mujer a partir de la pubertad, al igual que en la masculinización completa de los hombres.
Estas
características segundarias de ambos sexos estar regidas por la acción
hormonal.
Estas 5 etapas
que van en cascada secuencia en el desarrollo normal sexual de un individuo,
nos servirá para saber más afondo la biología y funcionamiento de nuestro cuerpo, además de conocer en que
parte de estos 6 etapas esta la alteración patología asociada a la
diferenciación sexual.
GENES INVOLUCRADOS EN LA DIFERENCIACIÓN SEXUAL O HACER PARTE IMPORTANTE DE LA DIFERENCIACIÓN DE ÓRGANOS SEXUALES
Translocación del gen SRY

Gen SRY y
determinación del sexo:
· El cromosoma Y es el principal determinante
de la diferenciación sexual masculina, este cromosoma, presenta un factor
determinante testicular.
· El factor determínate testicular fue
conocido como el gen SRY, el cual se describió en 1990.
· EL gen SRY está localizado en el brazo
corto del cromosoma Y. el SRY tiene un papel fundamental, al estimular el
desarrollo de las células de sertoli de los precursores gonadales bipotenciales
a través de la acción de SOX9.
· EL factor de transcripción codificado por el
gen SRY, tiene solo un exón de 850 kilobases, además de esto su dominio
funcional (HMG), está constituido por 79 aminoácidos, y este se une al ADN para
dar inicio a la trascripción del gen
· En estudios realizados se encontró que
mediante la transcripción del gen SOX9, en los pliegues gonadales y los conductos metanefricos, se ha podio
activar el gen SRY, que están presenten
en las células del epitelio celomico, que son las precursores de las células de
sertoli, en cambio la expresión del gen WNT4 , determina el desarrollo aparente
de las células de Leydig
· En las mujeres la usencia del gen SRY y la presencia de dos XX, va a asegurar el
desarrollo de los ovarios.
· Si hay una mutación o delación en el gen SRY, va a dar lugar a una mujer con
cariotipo XY con disgenesia gonadal caracterizado por genitales internos y
externos femeninos.
· Si hay una translocación de una parte del
cromosoma Y, en donde esté presente el gen SRY, al cromosoma X causara el síndrome masculino XX
Investigaciones realizadas en el departamento
de pediatría en la universidad de
colorado, Estados unidos, se
estudió la importancia del gen SOX9, y concluyeron, que si bien el gen sry es el interruptor inicial, del
desarrollo testicular, se sabe ahora que este gen es innecesario, si la
expresión del gen SOX9 es regulado incluso en su ausencia, como se puede
observar en duplicaciones de segmentos reguladores del gen SOX9, además se han encontrado otros
genes que regulan la expresión del Gen SOX9, como el gen SOX3 y lo hace en
ausencia del gen SRY.
Duplicación del gen SOX9

El SOX9 gen
contiene instrucciones para hacer una proteína, que juega un papel fundamental
durante el desarrollo embrionario. La proteína SOX9 es especialmente importante
para el desarrollo del sistema esqueleto y reproductivo. Esta proteína se une a
regiones específicas de ADN y regula la actividad de otros genes. Sobre la base
de esta acción, la proteína SOX9 se denomina un factor de transcripción.19
· El SOX9 gen se localiza en el brazo largo de cromosoma 17 en la posición 23( 17q23
· El gen SOX9 tiene una gran relación con
el gen SRY, si hay un mal funcionamiento del gen SOX9, puede causar anomalías
en la diferenciación sexual.
· Otras funciones importantes del gen SOX9 es
responsable de la maduración de los condrocitos, generando alteraciones
esqueléticas, produciendo displasias
campomelicas, que es causado por una mutación que va a afectar la dimerización , impidiendo hacer su función
cuando este se une al ADN. Si hay alguna mutación en una copia del gen SOX9, no
se producirá la transcripción del gen COL2A, que es el encargado de producir
colágeno tipo II normal en el hueso, y generara un colágeno anormal,
produciéndose una haploinsuficiencia. Se han encontrado más de 45 mutaciones en
el gen SOX9 que producen displasia campomelica.21
· Se han encontrado además mutaciones en el gen SOX9 en casos de
síndrome de Pierre-Robin.
· Debido a que el gen SOX9 tiene muchas
funciones en diferentes tejidos, principalmente durante la embriogénesis, sus
regiones reguladoras deberán ser muy complejas, se han encontrado que grandes
deleciones en secuencias precursores del gen SOX9, producirá displasia
campomelico o anormalidades en la
diferenciación sexual, o grandes
duplicaciones de las secuencias reguladoras causaran anoniquia- braquidactilia,
o duplicaciones pequeñas dentro de elementos reguladores pueden causar casos
aislados de anormalidades en la diferenciación sexual 46XX y deleciones
pequeñas causaran anormalidades de diferenciación sexual 46XY.21
Como se explicó
en el gen SRY, el gen SOX9, es de gran importancia en el desarrollo de las
células de sertoli, pero además de ello también influye en la regulación de la
expresión de AMH ( hormona anti-mulleriana
R-SPONDIN-1:
Es una proteína secretada, que en los seres
humanos esta codificada por el gen RSPO1
que se encuentra en el cromosoma 1. En los seres humanos interactúa con WNT4 en el proceso de desarrollo sexual femenino.
La pérdida de función hace que el desarrollo sexual femenino cambie a un
desarrollo sexual masculino.
· Se sabe que por medio de muchas
investigaciones que los genes SRY, y SOX9 son de gran importancia en el
desarrollo sexual masculino, pero en cambio las vías moleculares encargadas de
la diferenciación ovárica no eran muy claras, se pudo a través de grandes
estudios entre ellos el realizado en la universite de Nice-Sophis, laboratorio
de genetigue du Developpement et pathologigue normal, Niza, Francia, en su
artículo GENETICS OF OVARIAN DIFFERENTIATION: RSPO1, A MAJOR PLAYER. en este
estudio se encontró que el gen RSPO1 se
encuentra predominantemente expresado en las células somáticas de las gónadas
XX, en cambio en XY , el gen RSPO1 solo se expresa en el epitelio celomico.23
· Estudios en centraron que la ablación del
gen RSPO1, desencadena la reversión del sexo en los ratones XX, con la
formación de ovotestis y hermafroditismo de los genitales internos.
· Los estudios realizados en el artículo
anterior, encontraron que el fenotipo de los ratones XX con el gen RSPO1
muestra similitudes con la expresión del gen WNT4, lo que pude
sugerir que las mutaciones en estos dos genes van a actuar en la misma vía
molecular, además de que el gen WTN4 en parte está regulado por la acción del
gen RSPO1, que permite la regulación gonadal XX, otro gen encontrado y que
también depende de la presencia del gen RSPO1 es el gen WNT9.
· De acuerdo a los datos realizados en vitro
en ratones se encontró que el gen RSOP1, actúa en la vía de señalización
canonica en el desarrollo de los ovarios, además se observó en los ratones que
los genes RSPO1 y WNT4 antagonizar
la formación del testículo por
regulación a la baja de la
expresión SOX9 a través de la
inhibición de la activación de SF1 a TESCO y adema el gen WNT4 también
antagoniza Fgf9, un gen que se requiere para la expresión del gen SOX9.
La
determinación del sexo es debido a un equilibrio entre dos vías antagonistas,
mientras que el gen SRY estimula la expresión del SOX9, lo cual conducirá a la
diferenciación masculina, el gen RSPO1 inducirá la expresión del gen WNT4 y
promueve la canónica WNT / BETA CATENINA Y señalizacion ayudara en el
desarrollo sexual femenino.
HSD3B2
· La proteína codificada por este gen es una
enzima bifuncional que cataliza la conversión oxidativa de delta (5)-eno-3-beta-hidroxi-esteroide, y la
conversión oxidativa de cetosteroides. Juega un papel crucial en la biosíntesis
de todas las clases de esteroides hormonales. Este gen se expresa predominantemente
en las glándulas suprarrenales y las gónadas. Las mutaciones en este gen están
asociadas con deficiencia de 3-beta-hidroxiesteroide deshidrogenasa de tipo II.
En La literatura se han encontrado más de 37 mutaciones en el gen que causa la
deficiencia HD3B2-3- beta HSD.
· La 3 beta –hidroxiesteroide
deshidrogenasa es una enzima que tiene como función, catalizar la síntesis de
la progesterona, la 17-hidroxiprogesterona y la androstenediona. Esta es la
única enzima de las vías suprarrenales encargadas de la síntesis de corticoides
que no es miembro de la super familia de citocromo p450.
· Esta enzima convierte la pregnenolona
a progesterona, que es de gran
importancia durante el ciclo menstrual, debido a que ayuda a parar los cambios
del endometrio inducidos por los estrógenos, también ayuda a promover la
gestación, preparando al endometrio para la implantación del embrión y tiene
un papel en la embriogénesis. Una
función muy importante de la progesterona es
que ayuda en el desarrollo de las características segundarias en las
mujeres.
· La deficiencia de 3-beta
–hidroxiesteroide deshidrogenasa tipo 1 es una causa poco común de hiperplasia suprarrenal congénita.
Gen por deficiencia de P450 oxido reductasa.
· Se ha descrito un cuadro clínico de
genitales ambiguos y virilizacion
materna durante la gestación
debido a mutaciones en el gen de
la p450 oxido-reductasa (POR 7q11-2) que producirá no solo deficiencia parcial
mixta de 17alfa hidroxilasa y 21 alfa
hidroxilasa, sino también deficiencia de
aromatasa placentaria (responsable de la virilizacion materna).
Gen WNT4

· El gen WNt4 juega un papel muy importante
para determinación y diferenciación sexual femenina, además de esto atribuye al
mantenimiento de los ovarios y la
supervivencia de los folículos.
· El gen WNT4 codifica una proteína de
señalización extracelular, que tiene la
función de estimular la actividad de otros genes como la beta-catenina y
el factor lcf, es conocida por estar implicada en múltiples procesos del
desarrollo como la formación de los riñones,
las glándulas suprarrenales y las gónadas.
· La inactivación del gen, lleva a la
persona a la disgenesia ovárica con la producción temprana de testosterona por
las células mesenquimales y la formación de genitales internos masculinos,
incluyendo túbulos testiculares y las espermatogonias. El gen WNT4 se expresa
en la gónada embrionaria bipotencial en ambos sexos y se incrementa cuando se
forman pequeños folículos primarios, durante la mitad del embarazo. El ARNm del
gen WNT4 y su proteína están presentes
en los ovarios humanos.
· Otros estudios de investigación, demostraron
que la duplicación del gen WNT4, origina la reversión sexual 46XX en el humano.
· Durante el desarrollo del sistema
reproductor femenino, la proteína WNT4 regula la formación del conducto de
Müller, una estructura presente en el embrión que se desarrolla en el útero,
las trompas de Falopio, cuello uterino y la parte superior de la vagina. Esta
proteína también regula la producción de hormonas sexuales masculinas
(andrógenos) y el desarrollo y mantenimiento de los ovarios.
· Se encontró en un artículo, Desarrollo
femenino en los mamíferos está regulado por señalización Wnt-4, en el
nacimiento y desarrollo en los hombres
con una mutación en el gen WNT4 parece normal, sin embargo mujeres se mutan y
se masculinizan, el conducto de Müller está ausente mientras el conducto de
Wolff continua desarrollando.
· En un artículo realizado por S. Domenice,
sobre Mutations in the SRY, DAX1, SF1 and WNT4 genes in Brazilian sex-reversed
patients, se encontró, que debido a que el gen WNT4 está involucrado en el
desarrollo gonadal , también deberá estar presente y expresarse en los mesonefro
en desarrollo.
· En el estudio de Austin Larson, Disorders
of Sex Development: Clinically Relevant Genes Involved in Gonadal
Differentiation, Published on November 23, 2012, se pudo observar una pérdida de función en la mutación
heterocigota en el gen WNT4, al reportar un individuo con 46XX, el cual
presentaba fenotípicamente ausencia de útero, presencia de ovarios ectópicos y
displasicos e hiperandrogenismo, también se observó un paciente con duplicación
del cromosoma 1p35 que resultara en la sobreexpresión de gen WNT4, además de
presentar anomalía en la diferenciación
sexual con presencia de cariotipo 46XY , y presencia de hipospadias severas,
testículos rudimentarios y fibrosos, y útero rudimentario.
Mientras que
las duplicaciones en el gen WNT4, causan anomalías en la diferenciación sexual
y las mutaciones de perdida de función heterocigota producen anomalías de
Müller en pacientes con cariotipo 46 XX, se ha encontrado que las mutaciones
homocigóticas causan un grupo grande de anomalías y hallazgos severos como el
síndrome de serkal que es incompatible con la vida, entre los hallazgos
encontrados esta la agenesia renal, de corazón y anomalías pulmonares y además de anomalías en la diferenciación
sexual XX ,ya sea con o testículo ovotestis presentes en la autopsia

Muchas gracias por el resumen!!
ResponderEliminar